Единица измерения жесткости воды: перевод градусов и нормы жесткости воды. Таблицы значений, умягчение и удаление жесткости воды — Инженерный справочник DPVA.ru / Технический справочник ДПВА
Жесткость воды — важный показатель, который влияет на качество воды и может повлиять на работу бытовой техники. В этой статье мы рассмотрим единицы измерения жесткости воды, нормы жесткости воды и методы умягчения воды. — Инженерный справочник DPVA.ru / Технический справочник ДПВА.
Жесткость воды. Мягкая вода. Жесткая вода. Перевод единиц (градусов) жесткости воды. Нормы жесткости воды. Таблицы значений жесткости воды. Умягчение воды. Как убрать жесткость воды.
- жёсткой называется вода с большим содержанием солей ,
- мягкой с малым содержанием
"Жёсткая" вода — исторически: ткань, постиранная с использованием мыла на основе жирных кислот в жёсткой воде — более жёсткая на ощупь. Этот факт объясняется, с одной стороны, отложением на ткани кальциевых и магниевых солей жирных кислот, образующихся в процессе стирки. С другой стороны, волокна ткани обладают ионообменными свойствами, и, как следствие, свойством сорбировать многовалентные катионы — на молекулярном уровне.
- временная (карбонатная) жёсткость, — обусловлена гидрокарбонатами кальция и магния Са(НСО3)2; Mg(НСО3)2,
- постоянная (некарбонатная) жёсткость — вызванную присутствием других солей, не выделяющихся при кипячении воды: в основном, сульфатов и хлоридов Са и Mg (CaSO4, CaCl2, MgSO4, MgCl2).
С 1 января 2014 года в России введен межгосударственный стандарт ГОСТ 31865-2012 «Вода. Единица жесткости». По новому ГОСТу жесткость выражается в градусах жесткости (°Ж). 1 °Ж соответствует концентрации щелочноземельного элемента, численно равной 1/2 его миллимоля на литр (1 °Ж = 1 мг-экв/л). В разных странах использовались (иногда используются до сих пор) различные внесистемные единицы — градусы жёсткости.
Нормы жесткости воды — в 99,99% случаев речь идет о временной жесткости, данные ВСТ:
|
Жесткость воды, принятая в РФ |
Жесткость воды по нормам США |
||||||||
|
Категории |
°Ж = |
°dGH |
ppm = мг/л |
gpg |
°Ж = |
°dGH |
ppm = мг/л |
gpg |
|
|
1. Мягкая вода |
< 2 °Ж |
< 5,608 °dGH |
0 — 100 |
Мягкая вода = Soft water |
< 1,2 °Ж |
< 3,361 °dGH |
0 — 60 |
0 — 3.5 |
|
|
2. Вода средней жесткости |
2-10 °Ж |
5,608 — 28,04 °dGH |
100-500 |
Вода средней жесткости = Moderate hardness water |
1,2-2,4 °Ж |
3,361 — 6,724 °dGH |
61 — 120 |
3.5 — 7 |
|
|
3. Жесткая вода |
> 10 °Ж |
>28,04 °dGH |
>500 |
Жесткая вода = Hard hardness water |
2,4 — 3,6 °Ж |
6,724-10,085 °dGH |
121 — 180 |
7 — 10.5 |
|
|
— |
— |
— |
— |
— |
Очень жесткая вода = Very Hard hardness water |
> 3,6 °Ж |
> 10,085 °dGH |
> 180 |
> 10.5 |
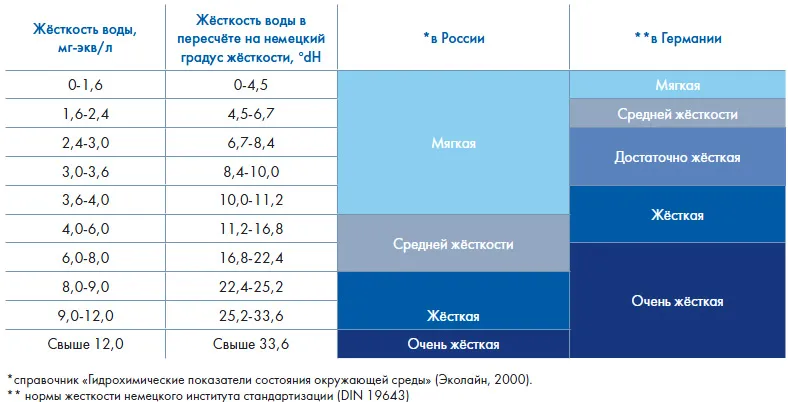
Сравнение принятных норм жесткости воды в РФ и Европе (Германии), данные Эколайн:
Жесткость воды в некоторых городах мира — данные МВК — неизвестной достоверности 🙂
Нормативные требования и рекомендации
- Рекомендации всемирной организации здравоохранения (ВОЗ) для питьевой воды:
- кальций – 20-80 мг/л; магний – 10-30 мг/л. Для жесткости какой-либо рекомендуемой величины не предлагается. Московская питьевая вода по данным показателям соответствует рекомендациям ВОЗ.
- Российские нормативные документы (СанПиН 2.1.4.1074-01 и ГН 2.1.5.1315-03) для питьевой воды регламентируют:
- кальций – норматив не установлен; магний – не более 50 мг/л; жесткость — не более 7°Ж.
- Норматив физиологической полноценности бутилированной воды (СанПиН 2.1.4.1116-02):
- кальций – 25-130 мг/л; магний – 5-65 мг/л; жесткость – 1,5-7°Ж.
- По содержанию кальция и магния бутилированная вода высшей категории официально ничем не лучше воды из-под крана
Перевод единиц и градусов жесткости воды — в 99,99% случаев речь идет о временной жесткости:
| °Ж = 1 мг-экв/л |
mmol/L | ppm, mg/L | dGH, °dH | gpg | °e, °Clark | °fH | |
| 1 русский °Ж = 1 мг-экв/л это: | 1 | 0,5 | 50,05 | 2,804 | 2,924 | 3,511 | 5,005 |
|---|---|---|---|---|---|---|---|
| 1 ммоль/л = mmol/L это: | 2 | 1 | 100.1 | 5.608 | 5.847 | 7.022 | 10.01 |
| 1 американский° ppmw = mg/L = American degre: | 0,01998 | 0.009991 | 1 | 0.05603 | 0.05842 | 0.07016 | 0.1 |
| 1 немецкий° dGH, °dH это: | 0,3566 | 0.1783 | 17.85 | 1 | 1.043 | 1.252 | 1.785 |
| 1 американская популярная ед. gpg это: |
0,342 | 0.171 | 17.12 | 0.9591 | 1 | 1.201 | 1.712 |
| 1 английский °e, °Clark это: | 0,2848 | 0.1424 | 14.25 | 0.7986 | 0.8327 | 1 | 1.425 |
| 1 французский °fH это: | 0,1998 | 0.09991 | 10 | 0.5603 | 0.5842 | 0.7016 | 1 |
| Пример: 1 °Ж = 50,05 ppm |
- американские градусы жесткости воды, внимание тут два пункта:
- gpg = Grains per Gallon: 1 гран (0.0648 г) CaCO3 в 1 американском галлоне (3.785 л) воды. Поделив граммы на литры получаем: 17.12 мг/л СаСО3 — это не "американский градус", но очень употребляемая в штатах величина жесткости воды.
- американский градус = ppmw = mg/L = American degre: 1 часть CaCO3 в 1000000 частей воды 1мг/л CaCO3
- английские градусы жесткости воды = °e = °Clark: 1 гран (0.0648 г) в 1 английском галлоне (4.546) л воды = 14.254 мг/л CaCO3
- французские градусы жесткости воды (°fH or °f) (fh): 1 часть CaCO3 в 100000 частей воды, или 10 мг/л CaCO3
- немецкие градусы жесткости воды = °dH (deutsche Härte = "немецкая жесткость" может быть °dGH (общая жесткость) или °dKH (для карбонатной жёсткости)): 1 часть оксида кальция – СаО в 100000 частей воды, или 0.719 частей оксида магния – MgO в 100000 частей воды, что дает 10 мг/л СаО или 7.194 мг/л MgO
- русский (РФ) градус жесткости воды °Ж = 1 мг-экв/л: соответствует концентрации щелочноземельного элемента, численно равной 1/2 его миллимоля на литр, что дает 50,05 мг/л CaCO3 or 20.04 мг/л Ca2+
- ммоль/л = mmol/L: соответствует концентрации щелочноземельного элемента, численно равной 100.09 мг/л CaCO3 or 40.08 мг/л Ca2+
Методы устранения жесткости воды
- Термоумягчение. Основан на кипячении воды, в результате термически нестойкие гидрокарбонаты кальция и магния разлагаются с образованием накипи:
- Ca(HCO3)2 → CaCO3↓ + CO2 + H2O.
- Кипячение устраняет только временную (карбонатную) жёсткость. Находит применение в быту.
- Реагентное умягчение. Метод основан на добавлении в воду кальцинированной соды Na2CO3 или гашёной извести Ca(OH)2. При этом соли кальция и магния переходят в нерастворимые соединения и, как следствие, выпадают в осадок. Например, добавление гашёной извести приводит к переводу солей кальция в нерастворимый карбонат:
- Ca(HCO3)2 + Ca(OH)2 → 2CaCO3↓ + 2H2O
- Лучшим реагентом для устранения общей жесткости воды является ортофосфат натрия Na3PO4, входящий в состав большинства препаратов бытового и промышленного назначения:
- 3Ca(HCO3)2 + 2Na3PO4 → Ca3(PO4)2↓ + 6NaHCO3
- 3MgSO4 + 2Na3PO4 → Mg3(PO4)2↓ + 3Na2SO4
- Ортофосфаты кальция и магния очень плохо растворимы в воде, поэтому легко отделяются механическим фильтрованием. Этот метод оправдан при относительно больших расходах воды, поскольку связан с решением ряда специфических проблем: фильтрации осадка, точной дозировки реагента.
- Катионирование. Метод основан на использовании ионообменной гранулированной загрузки (чаще всего ионообменные смолы). Такая загрузка при контакте с водой поглощает катионы солей жёсткости (кальций и магний, железо и марганец). Взамен, в зависимости от ионной формы, отдаёт ионы натрия или водорода. Эти методы соответственно называются Na-катионирование и Н-катионирование.
- При правильно подобранной ионообменной загрузке жёсткость воды снижается при одноступенчатом натрий-катионировании до 0,05-0,1 °Ж, при двухступенчатом — до 0,01 °Ж.
- В промышленности с помощью ионообменных фильтров заменяют ионы кальция и магния на ионы натрия и калия, получая мягкую воду.
- Обратный осмос. Метод основан на прохождении воды через полупроницаемые мембраны (как правило, полиамидные). Вместе с солями жёсткости удаляется и большинство других солей. Эффективность очистки может достигать 99,9 %.
- Различают нанофильтрацию (условный диаметр отверстий мембраны равен единицам нанометров) и пикофильтрацию (условный диаметр отверстий мембраны равен единицам пикометров).
- В качестве недостатков данного метода следует отметить:
- — необходимость предварительной подготовки воды, подаваемой на обратноосмотическую мембрану;
- — относительно высокая стоимость 1 л получаемой воды (дорогое оборудование, дорогие мембраны);
- — низкую минерализацию получаемой воды (особенно при пикофильтрации). Вода становится практически дистиллированной.
- Электродиализ. Основан на удалении из воды солей под действием электрического поля. Удаление ионов растворенных веществ происходит за счёт специальных мембран. Так же как и при использовании технологии обратного осмоса, происходит удаление и других солей, помимо ионов жёсткости.
- Дистиляция: Полностью очистить воду от солей жёсткости можно дистилляцией.
В чем измеряется жесткость балки?
Жесткость балки — это ее способность сопротивляться изгибу под действием внешних нагрузок. Жесткость измеряется в единицах, называемых Н/м² или Па (паскаль), которые представляют собой единицы измерения давления. Жесткость балки также может быть выражена в кН/м² (килоньютон на квадратный метр) или в psi (фунтах на квадратный дюйм), в зависимости от системы измерения. Жесткость балки обычно определяется экспериментально с помощью тестов на изгиб, которые позволяют определить отношение между приложенной нагрузкой и деформацией балки.